今回は、医療機器の保険適用についての制度を解説していきます。これまで、医療機器開発に関わる制度として、医療機器の分類、プログラム医療機器、承認審査制度などについてみてきましたが、ここでは、保険診療に用いられる医療機器が、どのようにして保険適用を受けるのかについてみていきます。
1.医療保険制度の仕組み
本題の医療機器の保険適用の話に入る前に、まず、医療保険制度の全般について、簡単に触れておきます
医療保険制度とは、患者が保険医療機関等から診療サービスを受けると、保険医療機関等はその対価として「診療報酬」を患者及び保険者から受け取る制度です。これにより、患者は受けた診療サービスの一部(原則3割、小児2割、高齢者は2割又は1割)を保険医療機関に直接支払い、残額は保険者により支払われます。
この保険の仕組みは、患者/被保険者(企業等の従事者の場合は企業等と折半、一部公費も投入)は、保険者(自治体、協会けんぽ、組合健保等)に保険料を支払います。一方、保険医療機関(病院、診療所、調剤薬局等)は提供した診療サービスの診療報酬を、審査支払機関(社会保険診療報酬支払基金、国民健康保険団体連合会)を介して、保険者に請求して診療報酬の支払を受けるというものです。
このように公的医療保険制度であるため、診療報酬は診療サービス(診療行為等)、サービス単価、請求要件(施設基準、算定要件)から厳格に定められ、点数化(1点10円)されています。
そして、報酬は主に、施設管理料、医師等の技術料、薬剤料、医療機器使用料に適用されています。
2.保険医療材料制度とは
医療機器には多種多様なものがあり、それらは、機械器具が84、医療用品が6、歯科材料が9、衛生用品が4、プログラムが3,プログラムを記録した記録媒体が3に分類されることが薬機法において定められていることは、その1で解説いたしました(リンク)。
保険適用をうける医療機器は「保険医療材料」と呼ばれ、薬機法の分類とは別に、「A1(包括)」、「A2(特定包括)」、「A3(既存技術・変更あり)」、「B1(既存機能区分)」、「B2(既存機能区分・変更あり)」、「B3(期限付改良加算)」、「C1(新機能)」、「C2(新機能・新技術)」、「R(再製造)」及び「F(保険適用に馴染まないもの)」に区分されます(下図「保険適用手続1」参照)。

図の黄緑色の部分の「A1(包括)」、「A2(特定包括)」、「A3(既存技術・変更あり)」に該当する医療機器は、診療報酬のうち技術料の中に製品の価格が含まれている区分となります。そのため、該当する医療機器は保険適用は受けていますが、別途、医療機器の価格を保険請求ものではありません。具体的な製品例として、A1には縫合糸、注射針、チューブなど、A2には超音波検査装置、酸素ボンベ、脳波計などが該当します。A3は、A2の区分に近いが完全には合致せず、定義の変更が必要なものです。
次に、水色の部分の「B1(既存機能区分)」、「B2(既存機能区分・変更あり)」、「B3(期限付改良加算・暫定機能区分)」に該当する医療機器は、診療報酬の技術料には含まれず、機能区分*1ごとに評価されて、医療機器の保険請求価格が定められる区分です。B1は、技術料とは別に既存の機能区分により評価されますが、具体的な製品例として、冠動脈ステント、ペースメーカーなどがあります。B2は既存の機能区分の定義の変更等を伴うもの、B3は既存の機能区分に期限付改良加算を付すことにより評価するものとなっています。
オレンジ色の部分の「C1(新機能)」、「C2(新機能・新技術)」に該当する医療機器は、B1・B2・B3と同様に、診療報酬の技術料には含まれず、機能区分ごとに評価されて、医療機器の保険請求価格が定められる区分です。ただし、B1・B2・B3 とは異なり、既存の機能区分には該当しないため新たな機能区分が必要になります。そして、C1・C2 と認められると、新たな「機能区分」と保険償還価格が定められます。
紫色の部分の「R(再製造)」は、再製造単回使用医療機器の原型医療機器*2が既存の機能区分または暫定機能区分に属しており、C1・C2 には相当しないもので、再製造品としての新たな機能区分が必要なものです。
最後に灰色の部分は、保険適用を受ける事は妥当ではないと判断された品目のための区分です。
なお、B3、C1、C2、Rは中央社会保険協議会*3における了承が必要な評価区分となります。
3.医療機器の保険適用の流れ
薬事承認又は認証を受けた医療機器について保険適用を受けるには、保険適用申請(保険適用希望書を厚生労働大臣宛てに提出)をする必要があります。
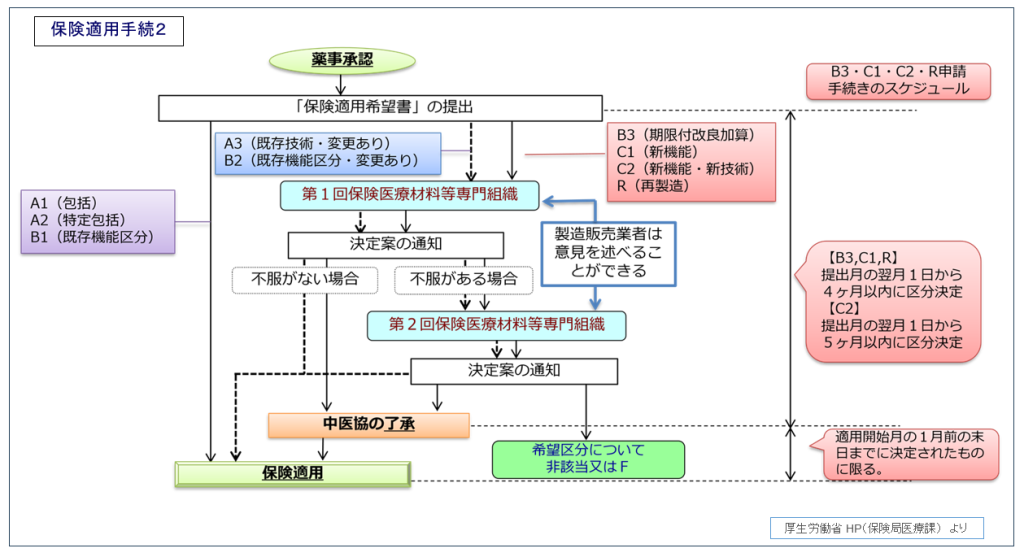
A1(包括)、A2(特定包括)、B1(既存機能区分)を希望する医療機器では、保険適用希望書を提出し受理されることで手続きは完了となり、希望通り保険適用することが適当と判断された医療機器については、保険適用となります。
A3(既存技術・変更あり)・B2(既存機能区分・変更あり)を希望する医療機器では、それぞれの区分に従って保険適用希望書を提出します。この保険適用希望書の審査に際して、必要に応じ申請企業からの意見聴取が行われます。その後、保険医療材料等専門組織*3の専門的見地からの検討を経て決定案が策定され、申請企業にその内容が通知されます。保険医療材料等専門組織による決定案に不服がある場合は、一度に限り不服申し立てを行うことができます。申請企業がこの決定案に同意すると、決定された月の翌月1 日から保険適用となります。
C1(新機能)・C2(新機能・新技術)・B3(期限付き改良加算・暫定機能区分)・R(再製造)を希望する医療機器では、それぞれの区分に従って保険適用希望書を提出します。これらについても、この保険適用希望書の審査に際して、必要に応じ申請企業からの意見聴取が行われます。その後、保険医療材料等専門組織の専門的見地からの検討を経て決定案が策定され、申請企業にその内容が通知されます。保険医療材料等専門組織による決定案に不服がある場合は、一度に限り不服申し立てを行うことができます。通知された内容に不服がない場合、中央社会保険協議会で審議・了承を得て保険適用となります。
申請から保険適用までの流れは以下のとおりです(下図「保険適用手続2」参照)。
4.新規機能区分の基準材料価格の算出方法
2で述べました「C1(新機能)」、「C2(新機能・新技術)」に該当する医療機器は、既存の機能区分には該当しないため、新たな開発・発明または構造・操作等の改良や工夫により既存の機能区分の定義(構造、使用目的、医療上の効能や効果等)と明らかに異なるものと認められると、新規収載品が属する機能区分として「新規機能区分」に分類されます。では、新規機能区分とされる医療機器の保険価格(基準材料価格)の算出方法についてみていきます(下図「保険適用手続3」参照)。
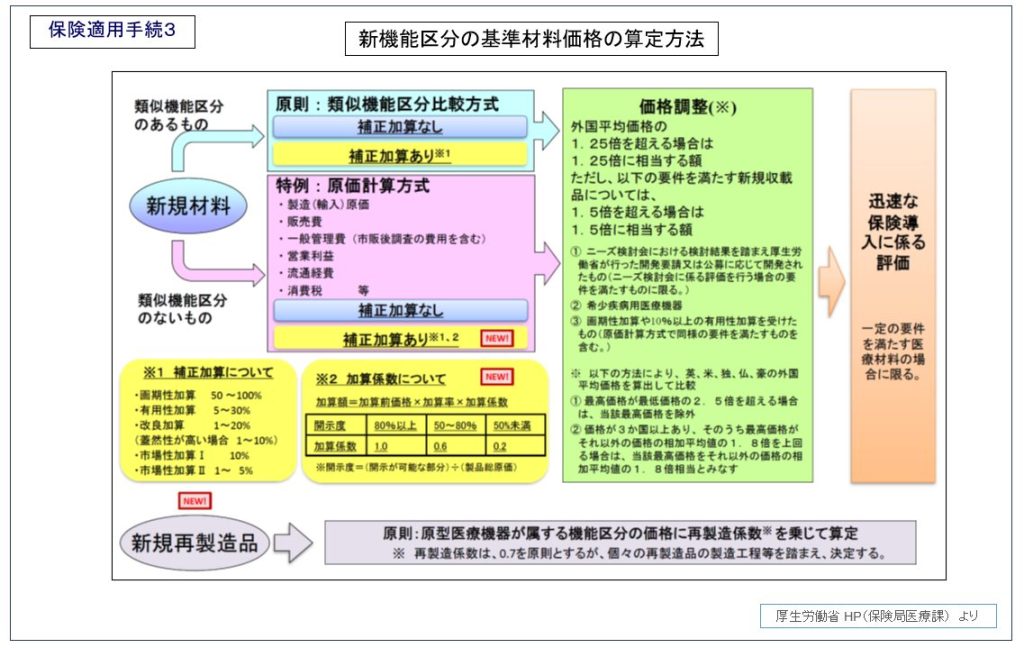
新規機能区分の基準材料価格の算出方法として、「類似機能区分比較方式」と「原価計算方式」の2 通りがあります。
「類似機能区分比較方式」とは、類似機能区分の基準材料価格を新規機能区分の基準材料価格とする方式のことで、原則、この「類似機能区分比較方式」で算定方法を用います。補正加算がある場合には、基本材料価格に画期的加算、有用加算、市場性加算などが加算されます。この価格を外国平均価格(英、米、独、仏、豪の平均価格から算出)と比較して価格調整がなされます。価格調整においては、希少疾病用医療機器、先駆的医療機器、特定用途医療機器、厚生労働省が行った開発要請に応じて開発されたことなどが考慮されます。更に、日本における薬事承認申請が米国における薬事承認申請より早いか又は180日以内であり、審査期間が一定以内である場合には、迅速な保険導入に係る評価が行われます。
「原価計算方式」とは、新規収載品の製造または輸入に要する原価に、販売費及び一般管理費、営業利益、流通経費、消費税及び地方消費税相当額を加えた額を当該新規収載品が属する新規機能区分の基準材料価格とする方式のことで、類似機能区分がない場合に用います。補正加算がある場合には、基本材料価格に画期的加算、有用加算、市場性加算などが加算され、開示度による加算係数*4が考慮されます。この価格以降の算定方法については、「類似機能区分比較方式」と同様です。
4. Other
(1)プログラム医療機器の評価について
プログラム医療機器の保険診療上の評価については、技術料に平均的に包括して評価されるもの、特定の技術料に加算して評価されるもの、特定の技術料に一体として包括して評価されるもの、特定保険医療材料として評価されるものがありますが、プログラム医療機器の評価を明確化する観点から、医科診療報酬点数表の医学管理等の部*5に、プログラム医療機器を使用した場合の評価に係る節が新設されました。
また、プログラム医療機器の特性から、医師の診療をサポートすることで、より少ない医療従事者で同等の質が確保できること等があり得ることから、プログラム医療機器の評価に当たっては、医師の働き方改革の観点を念頭に置きつつ、それぞれの製品の特性を踏まえ、施設基準等への反映も含め評価するとされています。
なお、保険導入を前提としておらず、患者の選択によるプログラム医療機器については、選定療養(保険外併用療養費制度)の仕組みの活用があり得ます。
(2)「チャレンジ申請」について
医療機器の中には、長期に体内に埋植するものや、革新性の高い技術を伴うもの等があり、保険収載までの間に最終的な評価項目を検証することが困難な場合があります。そのため、使用実績を踏まえた評価が必要な製品のうち、製品導入時には評価できなかった部分について、使用実績を踏まえて保険収載後に新規機能区分について再度評価を受けることができる制度(「チャレンジ申請」)があります。
従来は、対象品目が限定されていましたが、令和4年度保険医療材料制度の改定において、技術料に一体として包括して評価される医療機器等のうち、革新性の高い技術を伴うもの等についても、このチャレンジ申請の対象となりました。
今回は、医療機器の保険適用の制度についてみてきました。次回は、モバイルヘルス製品の保険適用について、具体的事例を解説していきます。
以上
*1:「機能区分」とは、構造、使用目的、医療上の効能及び効果等からみて類似していると認められる特定保険医療材料(保険医療機関等における医療材料の支給に要する平均的な費用の額が、診療報酬とは別に定められる医療材料)の一群として、厚生労働大臣が定める区分のこと。特定保険医療材料については、機能区分ごとに保険償還価格(基準材料価格)が定められている。特定保険医療材料については、機能区分ごとに保険償還価格(基準材料価格)が定められている。
*2:「再製造単回使用医療機器」とは、単回使用の医療機器のうち、使用後に検査、分解、洗浄、滅菌その他必要な処理を行うことにより再製造されたもので、原型医療機器と同等の品質、有効性及び安全性を有し、原型医療機器と使用目的又は効果が同様の医療機器のこと。
*3:「中央社会保険医療協議会(中医協)」とは、厚生労働省所管の審議会であり、診療報酬制度について審議がなされる。中医協には、専門部会・専門組織等があり、保険医療材料等専門組織は、平時は個々の特定保険医療材料等の保険適用について調査審議と改定時は機能区分の見直しを行っている。
*4:「開示度」とは、原価計算において、製品総原価に対する保険医療材料等専門組織での開示が可能な額の割合のことをいい、開示度が高いと加算係数が高くなる。
*5:「診療報酬点数表」とは、保険診療範囲を具体的に示した一覧表であり、「医科点数表」、「歯科点数表」、「調剤点数表」から成る。医科点数表の「第2章 特掲診療科 第1部 医学管理等」において、「第2節 プログラム医療機器等医学管理加算」が示されている。
参考:「特定保険医療材料の保険償還価格算定の基準について」(保発0209第3号令和4年2月9日)
「令和4年度医療機器・体外診断用医薬品の保険適用に関するガイドブック」
(令和5年3月 厚生労働省医政局医薬産業振興・医療情報企画課医療機器政策室)
Author: Tokuya Okanouchi
All rights reserved for this column.

Tokuya Okanouchi (CDI Medical Co., Ltd.)Managing Consultant)
Completed Graduate School of Pharmaceutical Sciences, Shizuoka Prefectural University, Completed Law School at Toin University of Yokohama, and completed Business School at the University of Massachusetts Lowell. Doctor (Pharmacy), Doctor of Law, MBA (Master of Business Administration)
After working at the Ministry of Health, Labor and Welfare, the National Hospital Organization, the Pharmaceuticals and Medical Devices Agency, the National Institute of Health Sciences, the Ministry of the Environment, the Ministry of Justice, and Kanagawa Prefecture.